Anwendungsinformationen
Fluoreszenz in der PCR-Diagnostik
Die PCR-Diagnostik ermöglicht es, DNA nachzuweisen und zu sequenzieren. Die RT-PCR wird verwendet, um RNA zu detektieren bzw. sequenzieren. Hierfür wird in einem ersten Schritt die RNA mit Hilfe der reversen Transkritase in DNA übersetzt um, sie dann bei der Polymerase-Kettenreaktion (Polymerase Chain Reaction, PCR) zu vervielfältigen. Schließlich werden die DNA-Abschnitte sequenziert. Klicken Sie auf den Artikel, um mehr zu erfahren...
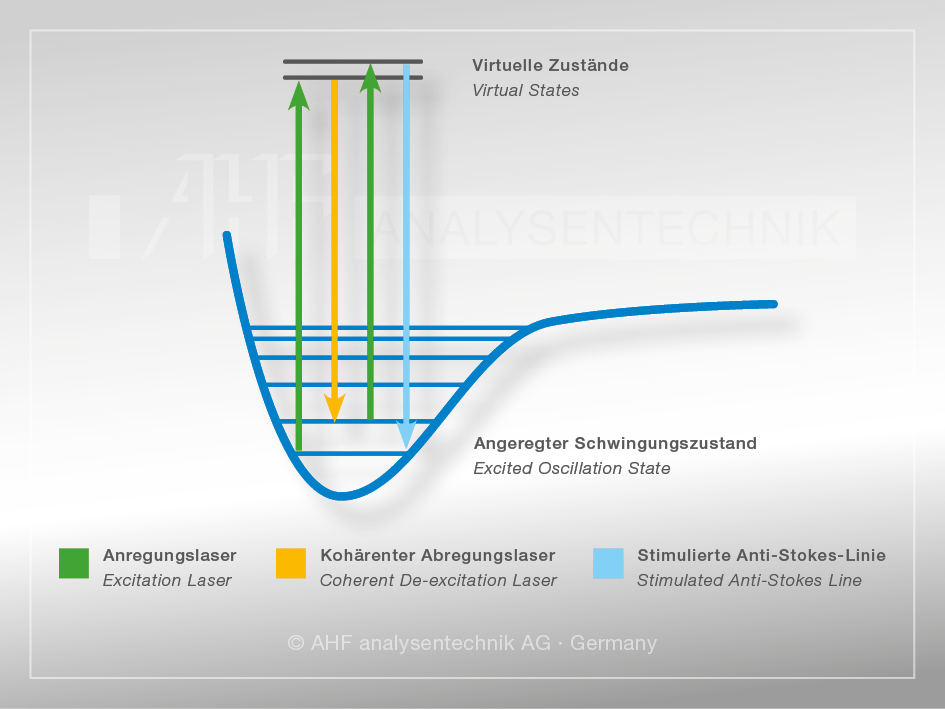
CARS-Mikroskopie
CARS steht für Coherent Anti-Stokes Raman Scattering. Es handelt sich um eine nichtlineare Raman-Spektroskopiemethode, bei der nicht nur mit einem Anregungslaser gearbeitet, sondern mit einem zweiten, rotverschobenen Laser die Probe bestrahlt wird.
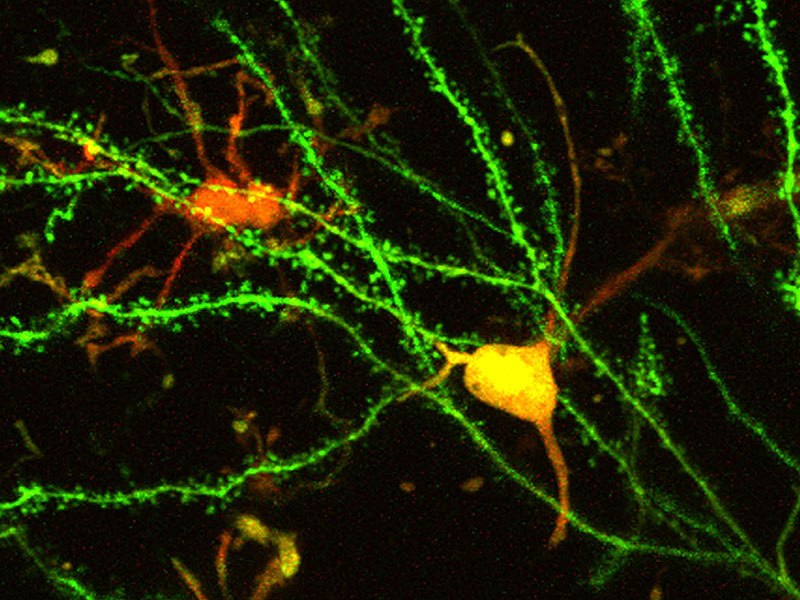
Die Multiphoton-Fluoreszenzmikroskopie
Bei der Multiphotonen-Mikroskopie werden Moleküle durch mehrere Photonen in einen elektronisch angeregten Zustand überführt. Von diesem Zustand relaxieren diese Moleküle durch Emission eines Photons wieder in den elektronischen Grundzustand. Dies hat zur Folge, dass das emittierte Photon eine höhere Energie (kürzere Wellenlänge) besitzt als die Photonen zur Anregung.
Filter-Tipps vom Profi: Signalstörungen in optischen Systemen beheben
Strahlverzerrung, Geisterbilder, störende Hintergrundsignale oder Untergrundstrahlung sind Probleme, die bei Anwendern in der Optik und Photonik, der Fluoreszenzmikroskopie, der hochauflösenden Mikroskopie oder bei der Entwicklung von Handheld-Systemen als sehr störend wahrgenommen werden. Wir zeigen Ihnen, was Sie tun können.
TIRF-Mikroskopie
Die TIRF-Mikroskopie (Total Internal Reflections Fluorescence Microscopy) ist eine Spezialanwendung der (Fluoreszenz-) Konfokalmikroskopie. Bei der TIRF-Mikroskopie wird in der Regel ein Objektiv mit hoher numerischer Apertur (NA) verwendet.
Eine kurze Einführung in die Super-Resolution-Mikroskopie
Unter hochauflösender Mikroskopie bzw. „Super-resolution Microscopy“ oder „Imaging“ versteht man in der Regel alle mikroskopischen Verfahren, die in der Lage sind, unterhalb der Beugungsgrenze aufzulösen.
Raman-Spektroskopie
Mit Raman-Spektroskopie werden, ähnlich wie bei der IR-Spektroskopie, Schwingungs- und Rotationsübergänge von Molekülen gemessen (mit anderen Auswahlregeln). Der Unterschied besteht darin, dass man bei der Raman-Spektroskopie kein IR-Licht verwendet, sondern sichtbares Licht. Dies ermöglicht es Detektoren und Optiken zu benutzen, die standardmäßig in der Optik verwendet werden.
STED-Mikroskopie
Die STED-Mikroskopie (STED = Stimulated Emission Depletion) als hochauflösende, im Scan-Modus arbeitende Methode stellt besondere Bedingungen an die Beschaffenheit ihrer optischen Komponenten.
Konfokalmikroskopie mit Laser
Die Konfokalmikroskopie ist eine spezielle Art der Lichtmikroskopie, bei der eine Probe punktweise abgerastert wird und anschließend diese Punkte Pixel für Pixel auf einem Computer zu einem Bild zusammengesetzt werden.
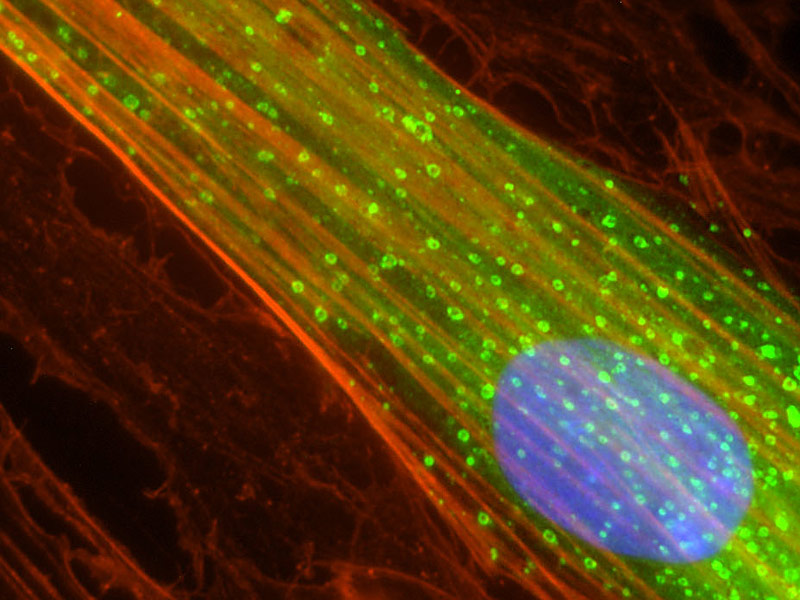
Fluoreszenzmikroskopie
Die Fluoreszenzmikroskopie hat sich wegen ihrer Vorteile bei Kontrast, Selektivität und Einfachheit der Einfärbung weltweit durchgesetzt und findet insbesondere in den Lebenswissenschaften (Life Sciences) häufig Anwendung. Hier stellen wir Ihnen diese spezielle Form der Lichtmikroskopie kurz vor.
FRET-Mikroskopie
Die "Förster- (oder auch Fluoreszenz-) Resonanzenergietransfer-Mikroskopie" ist eine Spezialanwendung der Fluoreszenzmikroskopie. Beim FRET-Effekt wird Energie von einem Donor-Molekül auf ein Akzeptor-Molekül übertragen. Die Effizienz dieses Energieübertrags nimmt mit der sechsten Potenz des Abstandes ab und ist auch abhängig von der Orientierung der Moleküle. Durch diese starke Entfernungsabhängigkeit kann man sehr genau Distanzen von 0 bis ca. 10 nm optisch vermessen.
STORM-Mikroskopie
STORM steht für STochastic Optical Reconstruction Microscopy. Dabei handelt es sich wie bei PALM (Photoactivated Localisation Microscopy) und GSDIM (Ground-State-Depletion and Individual Molecule return) und vielen anderen ähnlichen Methoden um Einzelmolekül-Lokalisationsmethoden die im Weitfeld-Modus arbeiten.